Covid: esquadrão de laboratórios checará eficácia de dezenas de testes
Sem tempo, irmão
- Entidades laboratoriais se preocupam com variedade de testes de coronavírus
- Já são 33 aprovados pela Anvisa; mais de 100 foram submetidos a análise do órgão
- Estudo agora tentará identificar eficácia e pontos fortes de cada teste
- Anvisa fez concessões para aprovação de testes contra Covid-19, dada a urgência
- Intenção do estudo é entender como cada teste reage em diferentes fases da infecção
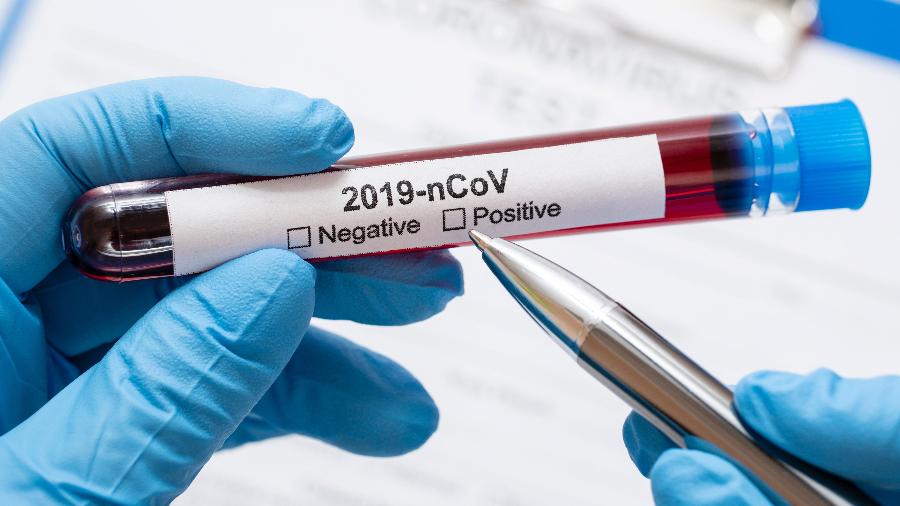
Desde o início da pandemia do coronavírus, 33 testes dos mais variados tipos para detecção da covid-19 foram aprovados pela Anvisa (Agência Nacional de Vigilância Sanitária). No total, 126 testes diferentes submeteram registro à agência até segunda (13). Com tantos tipos de testes no mercado, agora um grupo de laboratórios ajuda a Anvisa a entender sua real eficácia.
Com a entrada de vários kits no mercado, a iniciativa de validar os testes agora é liderada por instituições como Abramed (Associação Brasileira de Medicina Diagnóstica), a CBDL (Câmara Brasileira de Diagnóstico Laboratorial), a SBAC (Sociedade Brasileira de Análises Clínicas) e a SBPC/ML (Sociedade Brasileira de Patologia Clínica e Medicina Laboratorial).
Eles contarão com auxílio de laboratórios como Einstein, Dasa, Fleury, Sabin, Hermes Padini e Emílio Ribas/CE (laboratório no Ceará) para antecipar possíveis problemas em testes.
Por causa da gravidade do momento, a Anvisa fez concessões para acelerar a aprovação desses produtos no Brasil. Normalmente, um produto fica 200 dias na agência até ser aprovado. No caso dos testes para coronavírus, o período caiu para 15 dias de análise.
Mas esses testes não têm validação da Anvisa, que aprova ou não o registro deles de acordo com os documentos dados pelo fabricante.
"Há uma avaliação que é criteriosa. Tanto que temos 33 aprovados, cinco reprovados e outros 39 em exigência técnica, em que pedimos mais informações. Mas toda essa validação é uma relação de confiança com o que a empresa passou para nós. A coleta do mercado é posterior", explica ao Tilt Leandro Rodrigues, gerente-geral de produtos e tecnologias para saúde da Anvisa.
Entre as flexibilizações feitas pela Anvisa estão:
- A celeridade do processo;
- O tamanho das amostras exigidas nos estudos (por conta de ser uma doença nova);
- A estabilidade dos testes (condição de armazenamento e afins).
"A iniciativa surgiu da necessidade de se ter alguma referência para todos os testes disponíveis hoje. O registro da Anvisa não garante qualidade. Criamos um programa para cumprir uma etapa muito importante de validar o que esta no mercado", explica Priscila Martins, diretora-executiva da Abramed, que cita problemas com testes sem eficácia na Espanha e Reino Unido.
Hoje, a Anvisa diz que suas equipes estão mobilizadas somente para analisar testes para coronavírus.
Como vai funcionar a validação
A validação funcionará de forma "voluntária" para as empresas que produzem os testes. Elas serão convidadas a enviá-los, mas as que não enviarem poderão ser vistas com desconfiança pelas entidades do setor.
A partir daí, será seguido um protocolo para entender duas particularidades de cada teste:
- especificidade: a chance de uma pessoa sem a doença que faça o teste ter seu teste normal (negativo).
- sensibilidade: a chance de uma pessoa doente que faça o teste ter seu teste alterado (positivo).
As empresas fabricantes ou importadoras de testes contam com estudos do tipo que apresentam para a Anvisa, mas as entidades analisarão os kits levando em consideração diversas etapas do vírus no organismo humano.
Para isso, será vital a participação dos laboratórios, já que eles contam com amostras colhidas de pacientes em hospitais em dias diferentes da infecção.
No estudo, o teste molecular RT-PCR, o primeiro que surgiu contra o coronavírus, será usado como "padrão ouro" de qualidade para controle. Um painel será montado com cerca de 40 amostras sabidamente negativas (anteriores à chegada do vírus no país) e as amostras positivas serão testadas de acordo com o dia da infecção do paciente.
"Com isso vamos submeter todo e qualquer kit a esse painel para entender a real eficácia do teste. A questão que temos que ver é da sensibilidade: quanto maior, mais chance de pegar casos positivos", aponta Carlos Gouvêa, presidente da CBDL.
A intenção é que os primeiros relatórios sobre a eficácia já comecem a ser divulgados a partir da próxima semana.
"Não existe teste ruim e nem teste perfeito"
A pesquisa, que será conduzida por cientistas, biólogos, biomédicos e farmacêuticos de laboratórios, será vital para entender o que pode estar por trás da resposta de um kit. Nos últimos dias, tem crescido o número de relatos de falsos negativos em testes feitos para coronavírus, que dão positivo em testes seguintes.
"Quando der negativo, o que significa o teste rápido? Primeira opção: pode ser negativo mesmo, e a pessoa não teve contato com o vírus. A segunda pode ser a janela imunológica: o vírus já esta nela, mas não deu tempo de ter a resposta imunológica. A terceira é que o vírus já circulou, já gerou anticorpo, mas tem tão pouco que não pegou", aponta Gouvêa.
Estamos diante de um organismo inovador, desconhecido e queremos ter um panorama dos diferentes testes comercializados para que eles sejam usados de forma correta dentro das suas características. Não existe teste ruim e nem teste perfeito
Carlos Gouvêa, presidente da CBDL.(Câmara Brasileira de Diagnóstico Laboratorial)
Diferentes testes podem ter diferentes resultados em fases diferentes da infecção. O de biologia molecular (RT-PCR), por exemplo, é o padrão ouro e mais caro, mas é possível detectar só até um período, já que na sequência seriam encontrados os anticorpos.
O mais básico e barato é o teste imunocromatográfico, que é uma fita sensibilizada com partes do vírus. Esse teste envolve uma gota de sangue do paciente e tem os primeiros resultados em dez minutos.
Outro teste é o de anticorpo, que pode dizer se a pessoa está sem a doença, se está no início, no meio ou se já passou pela Covid-19. Esse teste é considerado eficaz para grupos grandes de pessoas (os chamados testes missivos), e um estudo da Universidade Federal de Pelotas começará a fazer isso.
O plano das entidades não tem caráter regulatório, mas servirá para o mercado e a própria Anvisa se balizarem. A agência também faz acompanhamento dos testes no mercado por meio do INCQS (Instituto Nacional de Controle de Qualidade em Saúde), um braço da Fiocruz.
Como testar a população
Segundo especialistas, a saída a curto prazo para a crise é fazer testagem ampla e irrestrita na população para controlar e entender a epidemia. É isso que fazem países que controlaram a doença sem esmagar o sistema de saúde, como Alemanha, Coreia do Sul e outros.
No Brasil, há críticas aos poucos testes feitos e temores sobre subnotificação de casos. Uma das razões é a falta de insumos no país.
"Mesmo na biologia molecular tem uma competição enorme entre países, todo mundo brigando pelo mesmo produto. No caso dos testes rápidos, a China mudou diretrizes para liberação dos kits, exigindo mais documentos. Com isso, o volume esperado para essa semana caiu tremendamente", aponta o presidente da CBDL.
Outro problema está em relação aos locais em que os testes são feitos. Atualmente, eles têm se concentrado em laboratórios que têm sofrido com a demanda —alguns pacientes esperam mais de dez dias para saber o resultado do exame para coronavírus.
Uma estratégia proposta pela CBDL é de levar a realização de exames também para hospitais e farmácias. A única exigência seria a realização por um profissional capacitado —não poderia ser um autoteste como os de gravidez, HIV e glicose.
"Para levar adiante a testagem em massa, é preciso cooperação entre governo e sociedade civil com algum tipo de flexibilização. Os hospitais e farmácias poderiam fazer um grande esforço para testar não só nos seus próprios profissionais, mas também nas comunidades", aponta Gouvêa.
Outra solução seria usar empresas, assim como em campanhas de vacinação. Segundo Gouvêa, existem várias empresas do setor privado dispostas a organizar a testagem dos seus funcionários e de pessoas da comunidade em torno da empresa em questão.
SIGA TILT NAS REDES SOCIAIS
- Twitter: https://twitter.com/tilt_uol
- Instagram: https://www.instagram.com/tilt_uol/
- WhatsApp: https://uol.page.link/V1gDd
- Grupo no Facebook Deu Tilt: http://bit.ly/FacebookTilt

















ID: {{comments.info.id}}
URL: {{comments.info.url}}
Ocorreu um erro ao carregar os comentários.
Por favor, tente novamente mais tarde.
{{comments.total}} Comentário
{{comments.total}} Comentários
Seja o primeiro a comentar
Essa discussão está encerrada
Não é possivel enviar novos comentários.
Essa área é exclusiva para você, assinante, ler e comentar.
Só assinantes do UOL podem comentar
Ainda não é assinante? Assine já.
Se você já é assinante do UOL, faça seu login.
O autor da mensagem, e não o UOL, é o responsável pelo comentário. Reserve um tempo para ler as Regras de Uso para comentários.