Técnica acelera produção de célula programada para combater câncer; entenda
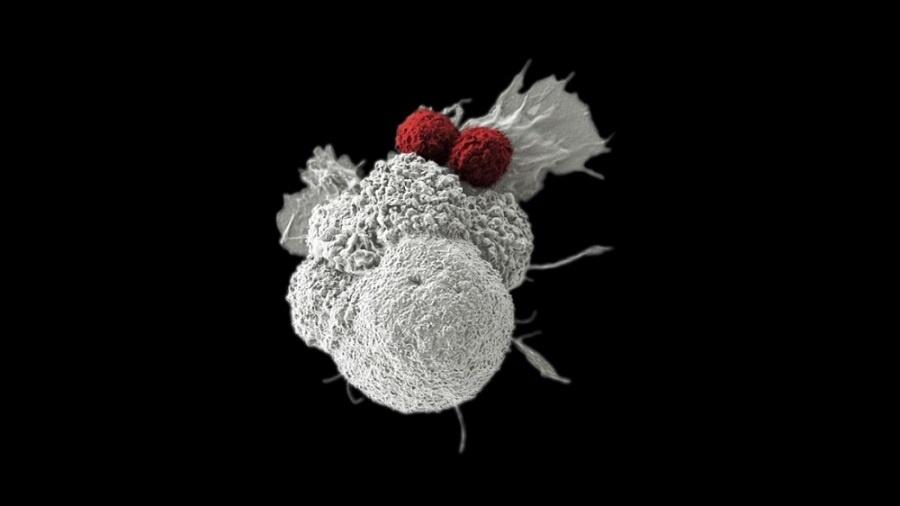
Pesquisadores do CTC-USP (Centro de Terapia Celular da Universidade de São Paulo) desenvolveram um método que reduz o tempo e o custo de produção das chamadas células T-CAR, uma das apostas atuais para o tratamento do câncer.
Essa tecnologia consiste em retirar células de defesa (linfócitos T) do paciente a ser tratado, reprogramá-las em laboratório para que reconheçam uma proteína chamada CAR (acrônimo em inglês para receptor de antígeno quimérico) e, assim, se tornem capazes de atacar o tumor. Essas células são então multiplicadas in vitro e reinfundidas no paciente.
Todo esse processo personalizado costuma demorar de duas a três semanas para ser concluído, o que pode ser um tempo longo para quem é portador de doença em estágio avançado. Além disso, nem sempre se consegue obter células em quantidade e qualidade necessárias para o tratamento.
Para contornar esses obstáculos, o grupo do CTC desenvolveu uma técnica que permite usar linfócitos T de doadores saudáveis não aparentados, modificar e expandir essas células em laboratório de modo a produzir múltiplas doses para tratar mais de um doente, reduzindo custos.
"Para usar essas células no tratamento de indivíduos não aparentados, algumas moléculas precisam ser removidas para evitar a rejeição. Nós usamos uma técnica inovadora de edição gênica chamada CRISPR/Cas9. Com ela, as proteínas Cas9 cortam o DNA em regiões que nós especificamos e, assim, as moléculas responsáveis pela rejeição não são mais produzidas. Além disso, nós aproveitamos os cortes feitos no DNA pela Cas9 para fazer uma segunda modificação, que consiste na inserção do gene codificador da proteína CAR", conta Sarah Caroline Gomes de Lima.
A cientista desenvolveu o método na Universidade de Wisconsin-Madison (Estados Unidos) durante estágio financiado pela FAPESP.
No Hemocentro de Ribeirão Preto, Lima desenvolve um projeto de mestrado sob a orientação de Lucas Eduardo Botelho de Souza, professor da FMRP-USP (Faculdade de Medicina de Ribeirão Preto) e integrante do CTC, um Centro de Pesquisa, Inovação e Difusão (CEPID) da FAPESP.
O estudo de Lima, intitulado "All-In-One Virus-Free Manufacturing Process of Allogeneic Chimeric Antigen Receptor (CAR) T Cells Using CRISPR-Cas9", foi selecionado como o "melhor trabalho de transplante de medula óssea e terapia celular" do Congresso Brasileiro de Hematologia, Hemoterapia e Terapia Celular (HEMO) de 2022.
Organizado pela Associação Brasileira de Hematologia, Hemoterapia e Terapia Celular, o evento ocorrerá entre 26 e 29 de outubro, no Transamerica Expo Center, em São Paulo
Mais detalhes sobre a pesquisa podem ser encontrados em vídeo produzido pela TV Hemocentro RP, disponível no YouTube.
Este texto foi originalmente publicado por Agência FAPESP de acordo com a licença Creative Commons CC-BY-NC-ND. Leia o original aqui.












ID: {{comments.info.id}}
URL: {{comments.info.url}}
Ocorreu um erro ao carregar os comentários.
Por favor, tente novamente mais tarde.
{{comments.total}} Comentário
{{comments.total}} Comentários
Seja o primeiro a comentar
Essa discussão está encerrada
Não é possivel enviar novos comentários.
Essa área é exclusiva para você, assinante, ler e comentar.
Só assinantes do UOL podem comentar
Ainda não é assinante? Assine já.
Se você já é assinante do UOL, faça seu login.
O autor da mensagem, e não o UOL, é o responsável pelo comentário. Reserve um tempo para ler as Regras de Uso para comentários.