Texto que relata acontecimentos, baseado em fatos e dados observados ou verificados diretamente pelo jornalista ou obtidos pelo acesso a fontes jornalísticas reconhecidas e confiáveis.
Lecanemab: remédio para o Alzheimer não deve dar certo, mas há um lado bom

Receba os novos posts desta coluna no seu e-mail
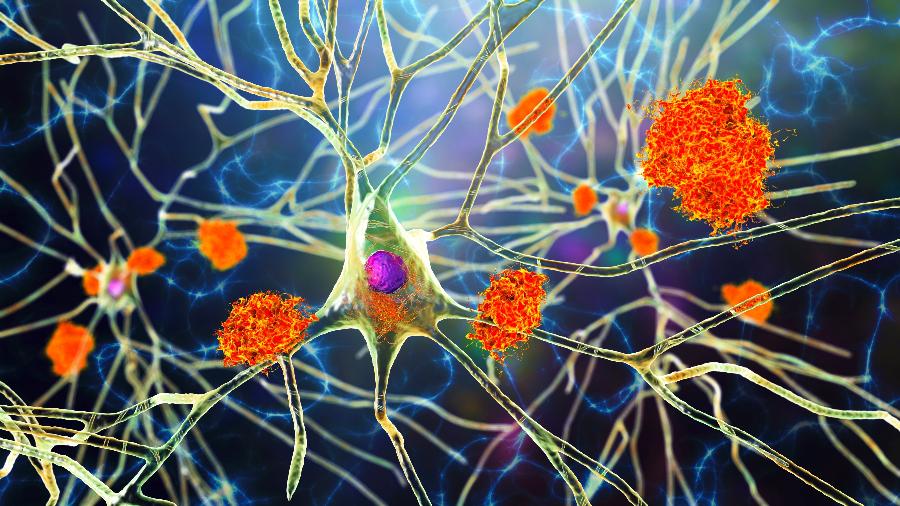
Acabou sendo um estardalhaço quando, há dez dias, em um evento sobre Alzheimer na Califórnia, nos Estados Unidos, foram anunciados os primeiros resultados de uma droga capaz de agir nas placas de proteína beta-amiloide que se formam no cérebro de quem tem a doença e reduzir o declínio da cognição e da memória.
Este, aliás, é o ponto: mostrar efeito sobre a cognição e não só em exames de imagem cerebral. Isso, sim, é inédito e pode valer algum barulho.
Cá entre nós, quem convive com o Alzheimer — um dos 50 milhões de indivíduos com esse apagão nos neurônios ao redor do mundo e seus familiares — conhece a gangorra da esperança e do desapontamento como ninguém.
O lecanemab, como se chama a molécula da vez, não é o primeiro medicamento que surge com a intenção de pelo menos frear a demência mais frequente que a humanidade já viu — frequente e crescente, já que serão 74,7 milhões de casos espalhados pelo globo daqui a apenas oito anos, de acordo com a Alzheimer's Disease International. E mais de 131 milhões em 2050.
A explosão é detonada pelo aumento da expectativa de vida e, consequentemente, do número de idosos em todos os cantos.
Nos últimos vinte anos, apareceram outras promessas com nomes esquisitos, difíceis para qualquer um gravar, como a bapineuzumab e a solanezumab que, nos ensaios clínicos em gente como a gente, foram um fiasco total.
Já em 2019, a esperança voltou a subir com o aducanumab, mas logo o desapontamento foi para as alturas e ainda chamou a polêmica para entrar na brincadeira, pois o remédio oferecia um risco considerável e não provou ter qualquer efeito sobre a função cognitiva. Mesmo assim, chegou a ser aprovado pelo FDA, a agência americana que regula medicamentos, levando funcionários a pedir demissão depois.
O lecanemab, diga-se, é um descendente direto dessa última droga que causou confusão. Nasceu no mesmo laboratório americano do aducanumab, o Biogen, desta vez em parceria com outra farmacêutica, a japonesa Eisai. Mas vamos tirar o chapéu: além de um pouco mais seguro, diferentemente de suas antecessoras ele pareceu diminuir o avanço do Alzheimer.
As outras drogas também miravam na beta-amiloide. Mas, depois, quando os cientistas avaliaram as funções cognitivas dos participantes dos estudos, viram que seus tiros tinham dado em água.
Daí que, quando o artigo sobre o lecanemab saiu no prestigiado New England Journal of Medicine, no mesmo dia 29 de novembro, em que rufaram os tambores no evento sobre Alzheimer, teve quem aplaudisse de pé. Alguns até falaram que a sua chegada seria "um divisor de águas". Mas calma: ainda estamos na gangorra.
"Isso pode despertar nas pessoas a impressão de que daqui para frente vai dar tudo certo", observa, preocupado com a esperança vã, o neurologista Diogo Haddad Santos, que coordena o Núcleo de Memória do Hospital Alemão Oswaldo Cruz, em São Paulo. "Esse seria um erro de interpretação", afirma.
Estudo versus realidade
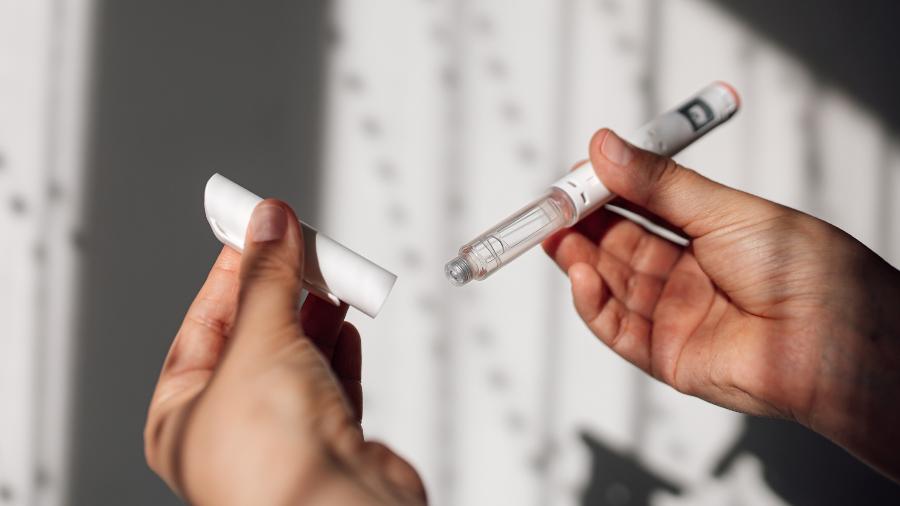
O lecanemab é, na realidade, um anticorpo monoclonal. Em outras palavras, uma molécula que imita os anticorpos do nosso sistema de defesa, mas desenhada em laboratório para atacar um alvo específico que, no caso, foram os pontos de acúmulo da proteína beta-amiloide atravancando a conversa entre os neurônios.
O estudo, assinado por cientistas de centros de diversos países, envolveu 1.795 indivíduos de 50 a 90 anos. Eles foram randomizados, isto é, sorteados. Sem ninguém saber se estava usando o remédio pra valer ou não, 898 deles caíram no grupo que recebeu a medicação na veia a cada duas semanas ao longo de 18 meses. E, no restante, os cientistas injetaram placebo, ou seja, um medicamento falso para fazer a comparação.
O que todas essas pessoas tinham em comum: as tais placas de beta-amiloide bem evidentes na cabeça e apenas um leve comprometimento cognitivo.
"Aí é que está: embora conte com um número grande de indivíduos, podemos dizer que o trabalho os escolheu sob medida para que seus resultados dessem certo", comenta Santos. "Isso porque, na prática, dificilmente encontramos um paciente que já tenha acometimento no cérebro e com uma doença assim tão leve."
Ou seja, os participantes estavam todos em uma fase de transição, à beira de manifestações mais claras do Alzheimer. Gente como, possivelmente, eu e você conhecemos, mas que ninguém sabe ainda que está com a doença neurodegenerativa. O remédio funcionaria se ela estivesse mais avançada? É mais provável que não.
Por que, na prática, resultado não muda nada
Na avaliação das funções cognitivas realizada nos participantes após os tais 18 meses, quem usou o medicamento viu a doença progredir 27% mais devagar. Parece ótimo, não? Mas lembre-se que ela estava no início. Se olhar direito, verá que os usuários do lecanemab melhoram em média apenas 0,45 ponto em uma escala de 18 pontos.
É sabido por essa metodologia de avaliação — clássica e respeitada nos meios científicos — que seria preciso a diferença de no mínimo 1 ponto para se notar qualquer mudança no dia a dia do paciente. Em casos de Alzheimer um pouco mais avançado, a diferença teria de ser de 1,6 ponto.
Pois é: a nota dos usuários do lecanemab não foi assim tão alta. Melhorou? Melhorou. Mas longe do suficiente.
Hemorragia e inchaço no cérebro
O medicamento provocou sangramentos em 17% dos participantes e edema, ou inchaço, cerebral em 13% deles. Outros 7% deixaram o estudo pelo caminho por causa dos efeitos colaterais. Aliás, depois da divulgação bombástica, veio à tona a notícia de dois sujeitos que morreram e ainda não se sabe se foi por causa do lecanemab.
"Os anticorpos monoclonais são usados há mais tempo em outras áreas da Medicina, como pelos oncologistas para combater tumores", comenta Santos. "Na neurologia, porém, seu emprego é muito recente e ainda estamos aprendendo quais seriam as reações."
Uma hipótese, segundo ele, é o anticorpo provocar uma leve inflamação ao combater uma proteína específica, daí o edema. "Todos nós temos beta-amiloide no cérebro", lembra. "E essa espécie de limpeza talvez agrave uma fragilidade vascular que já existisse antes."
Na opinião do médico, sangramentos no cérebro, por menores que sejam, são sempre um risco gravíssimo. Por isso, ele aposta que, em novas etapas de estudo com o lecanemab, os cientistas investiguem quem são os pacientes com vasos sanguíneos mais frágeis.
Mas a questão que volta é: diante de resultados tão tímidos somente na fase inicial do Alzheimer, vale a pena arriscar? Ela precisa ser posta à mesa, porque a novidade deverá ser analisada para aprovação pelo FDA no raiar de 2023, que já está aí, dobrando a esquina.
Placas de beta-amiloide sozinhas criam o Alzheimer?
Esta é mais uma pergunta importante. Quando o psiquiatra e neuropatologista alemão Alois Alzheimer (1864-1915) mostrou algo diferente no cérebro de um paciente com a doença que acabaria ganhando o seu nome, ele já apontou as tais placas.
"Impressionante como, 120 anos depois, ainda ficamos batendo só na tecla delas", nota Santos. "De fato, ainda conhecemos muito pouco sobre a fisiopatologia do Alzheimer." Sim, ele parece ser fruto de uma combinação de vários fatores. E, hoje se sabe, compromete muito mais do que a memória.
"Muitas vezes encontramos pacientes com déficits que têm a ver com regiões cerebrais onde nem placas de beta-amiloide encontramos nos exames de imagem", conta. "Portanto, há mais coisa aí."
Mais de um remédio
Isso leva ao pensamento de que as concentrações de beta-amiloide seriam apenas parte ou, quem sabe, um ponto de partida da doença.
"Interessante ver que pesquisas com agonistas do GLP-1, drogas usadas para tratar o diabetes, parecem retardar o avanço do Alzheimer", revela o médico para dar um exemplo, deixando claro que isso ainda precisa ser melhor investigado.
"Mas, se for verdade, é porque esses remédios diminuiriam a inflamação nos microvasos do cérebro, que também parece estar envolvida na degeneração dos neurônios", especula.
Onde ele quer chegar: no futuro, o Alzheimer não será tratado com um único medicamento atacando um alvo específico, como o anticorpo monoclonal faz com as placas anormais de proteína, mas por um punhado deles, cada um agindo em uma frente.
A maior dificuldade é que, em matéria de Alzheimer, a ciência mal engatinha para entender quais frentes seriam essas.
É justamente aí que está o lado bom de toda a barulheira em torno do lecanemab: ao agir em fases muito iniciais da doença, ele escancara a necessidade de se desenvolveram estratégias e exames para diagnosticá-la bem mais cedo.
"Se investirem nisso, além de pacientes de países como o Brasil serem beneficiados — pois temos outros fatores de risco, como a baixa escolaridade — certamente iremos compreender mais as origens do problema", pensa Santos. Sem essa compreensão, esqueça.












ID: {{comments.info.id}}
URL: {{comments.info.url}}
Ocorreu um erro ao carregar os comentários.
Por favor, tente novamente mais tarde.
{{comments.total}} Comentário
{{comments.total}} Comentários
Seja o primeiro a comentar
Essa discussão está encerrada
Não é possivel enviar novos comentários.
Essa área é exclusiva para você, assinante, ler e comentar.
Só assinantes do UOL podem comentar
Ainda não é assinante? Assine já.
Se você já é assinante do UOL, faça seu login.
O autor da mensagem, e não o UOL, é o responsável pelo comentário. Reserve um tempo para ler as Regras de Uso para comentários.