Vacina da Pfizer é segura para crianças de 5 a 11 anos, dizem fabricantes
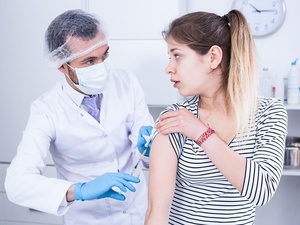
A Pfizer e a BioNTech anunciaram hoje que sua vacina contra a covid-19 induz a uma resposta imune robusta em crianças de 5 a 11 anos. O perfil de segurança do imunizante também é comparável com o da faixa etária entre 16 e 25 anos.
Com o fim dos ensaios clínicos de fase 2 e 3, as fabricantes planejam pedir autorização de uso da vacina em crianças às autoridades dos Estados Unidos até o o final mês. Em seguida, o pedido será encaminhado a reguladores europeus e britânicos.
"Desde julho, casos pediátricos de covid-19 aumentaram em cerca de 240% nos Estados Unidos —enfatizando a necessidade de saúde pública de vacinação", afirmou o presidente-executivo da Pfizer, Albert Bourla, em comunicado à imprensa.
Para crianças em idade escolar, a Pfizer testou uma dose muito mais baixa, um terço da quantidade que está em cada injeção dada agora. Mesmo assim, após a segunda dose, crianças de cinco a 11 anos desenvolveram níveis de anticorpos que combatem o coronavírus, disse o Dr. Bill Gruber, vice-presidente sênior da Pfizer, à Associated Press.
Pfizer e BioNTech também realizaram testes clínicos para entender como a vacina atua em crianças de entre 2 e 5 anos e em bebês de 6 meses a 2 anos. Os resultados devem ser divulgados até o 4º trimestre deste ano.
Em entrevista à CNN, o coordenador de testes da vacina Pfizer no Brasil, Cristiano Zerbini, ressaltou a importância da vacinação para crianças de 5 a 11 anos. "Elas precisam voltar à vida normal e temos que diminuir a circulação do vírus para que não surjam novas variantes".
Ele explicou que os testes de hoje foram comparados aos estudos clínicos em pessoas de 16 a 25 anos. O resultado foi "bastante semelhante" em termos de eficácia e segurança.
Nos estudos em crianças, os efeitos colaterais temporários foram semelhantes ou mais leves que os experimentados pelos adolescentes. Segundo Zerbini, houve relatos de dor no local da aplicação, dor de cabeça e fadiga, sintomas considerados leves e que desaparecem em até 7 dias.
O estudo
O estudo segue está em andamento e não houve casos de covid-19 suficientes entre as crianças analisadas para comparar as taxas entre os vacinados e aqueles que receberam um placebo.
Já a Pfizer afirma que assim que a vacina for autorizada para crianças mais novas, elas serão cuidadosamente monitoradas para riscos raros, assim como qualquer outra pessoa.
Autorização para uso da vacina
Nos Estados Unidos, diz a Reuters, autoridades de saúde de alto escalão acreditam que os órgãos reguladores decidirão se a vacina é segura e eficaz em crianças mais novas em até três semanas após a entrega dos pedidos de autorização de uso da vacina.
As internações e mortes por covid-19 saltaram nos Estados Unidos nos últimos meses devido à variante Delta do coronavírus, altamente contagiosa. Casos pediátricos da doença também estão em alta, particularmente porque crianças com menos de 12 anos não estão sendo vacinadas, mas não há nenhuma indicação de que, além de ser mais transmissível, a Delta seja mais perigosa para crianças.
Uma autorização rápida ajudaria a mitigar um potencial aumento de casos no outono do Hemisfério Norte, especialmente com as escolas já abertas em todo os EUA.
A vacina Pfizer já está autorizada para aplicação em crianças a partir de 12 anos em vários países, incluindo o Brasil.
Na semana passada, o ministro da Saúde, Marcelo Queiroga, afirmou que a pasta deixaria de recomendar a vacinação contra covid em adolescentes sem comorbidades até que haja mais evidências "sólidas".
No dia seguinte, a Anvisa (Agência Nacional de Vigilância Sanitária) anunciou que mantém a orientação de vacinar adolescentes, após se reunir com a Pfizer.
Em nota, a agência demorou que "os achados apontam para a manutenção da relação benefício versus o risco para todas as vacinas autorizadas no Brasil, ou seja, os benefícios da vacinação excedem significativamente os seus potenciais riscos".
Mesmo após a recomendação do Ministério da Saúde, ao menos 16 capitais e o Distrito Federal continuaram a vacinar adolescentes.
*Com Reuters e Estadão Conteúdo








ID: {{comments.info.id}}
URL: {{comments.info.url}}
Ocorreu um erro ao carregar os comentários.
Por favor, tente novamente mais tarde.
{{comments.total}} Comentário
{{comments.total}} Comentários
Seja o primeiro a comentar
Essa discussão está encerrada
Não é possivel enviar novos comentários.
Essa área é exclusiva para você, assinante, ler e comentar.
Só assinantes do UOL podem comentar
Ainda não é assinante? Assine já.
Se você já é assinante do UOL, faça seu login.
O autor da mensagem, e não o UOL, é o responsável pelo comentário. Reserve um tempo para ler as Regras de Uso para comentários.