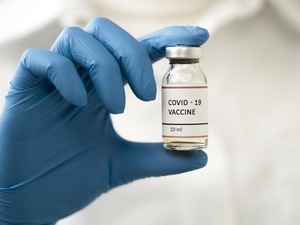
CoronaVac tem mínimo de infectados e Butantan espera aprovação em janeiro
O governo de São Paulo anunciou hoje que os estudos de fase três da CoronaVac, que podem atestar a eficácia da vacina contra a covid-19 desenvolvida pelo Instituto Butantan em parceria com o laboratório chinês Sinovac, chegaram ao número mínimo de infectados pelo novo coronavírus. Com essa marca, é possível abrir os resultados dos estudos para análise da aprovação do registro pela Anvisa (Agência Nacional de Vigilância Sanitária).
O Butantan trabalha com a expectativa de que a Anvisa possa conceder o registro da vacina até janeiro, o que já permite o início de uma campanha de vacinação contra a covid-19 no estado. Para isso, São Paulo deve ter 46 milhões de doses disponíveis, sendo seis milhões vindo já prontas da China e mais 40 milhões produzidas na fábrica do Butantan na capital. Na última quinta-feira (19), chegaram ao país as primeiras 120 mil doses da vacina.
Nos estudos de fase três do imunizante que são conduzidos no Brasil, 74 pessoas contraíram até agora o novo coronavírus de um total de 13 mil voluntários que irão participar dos testes. O mínimo para abrir os testes era de 61 infectados.
"A expectativa é que já no mês de janeiro a Anvisa tenha aprovado a CoronaVac e com 46 milhões de doses o Instituto Butantan, em conjunto com PNI [Programa Nacional de Imunizações], terá possibilidade de vacinar brasileiros de todo o país. A celeridade da CoronaVac vai permitir que a CoronaVac seja a primeira vacina disponível para a nossa população e, como sempre reforçamos, só com a vacina viveremos o nosso normal", afirmou hoje o secretário estadual de Saúde de São Paulo, Jean Gorinchteyn, durante entrevista coletiva na sede do Butantan em São Paulo.
O Butantan enviou as análises do estudo da CoronaVac ao comitê internacional para validação. É esta análise que determina a eficácia da vacina. Quando o documento voltar deste comitê, o que é esperado para a primeira quinzena de dezembro, ocorrerá a entrada no pedido de autorização na Anvisa.
O mesmo é feito com a agência reguladora chinesa, país do laboratório Sinovac. A expectativa da Secretaria estadual de Saúde de São Paulo é que a Anvisa termine sua avaliação até o começo de janeiro. As 46 milhões de doses da vacina então seriam suficientes para vacinar toda a população do estado paulista.
A expectativa de começar a vacinação no início de 2021 é compartilhada pelo diretor do Butantan, Dimas Covas. "Essas notícias colocam essa vacina como a vacina mais próxima de utilização aqui no Brasil. É a que está mais próxima de estar disponível para a população", afirmou.
Os testes da CoronaVac no Brasil acontecem desde julho em 16 centros de pesquisa científica espalhados por sete estados brasileiros e no Distrito Federal. Na China, os estudos de fase um e dois já foram concluídos e comprovaram eficácia superior a 90% do imunizante. Para o registro na Anvisa, é necessário que a vacina tenha pelo menos 50% de eficácia.











ID: {{comments.info.id}}
URL: {{comments.info.url}}
Ocorreu um erro ao carregar os comentários.
Por favor, tente novamente mais tarde.
{{comments.total}} Comentário
{{comments.total}} Comentários
Seja o primeiro a comentar
Essa discussão está encerrada
Não é possivel enviar novos comentários.
Essa área é exclusiva para você, assinante, ler e comentar.
Só assinantes do UOL podem comentar
Ainda não é assinante? Assine já.
Se você já é assinante do UOL, faça seu login.
O autor da mensagem, e não o UOL, é o responsável pelo comentário. Reserve um tempo para ler as Regras de Uso para comentários.