Como garantir a segurança e a distribuição de uma vacina contra a covid-19?
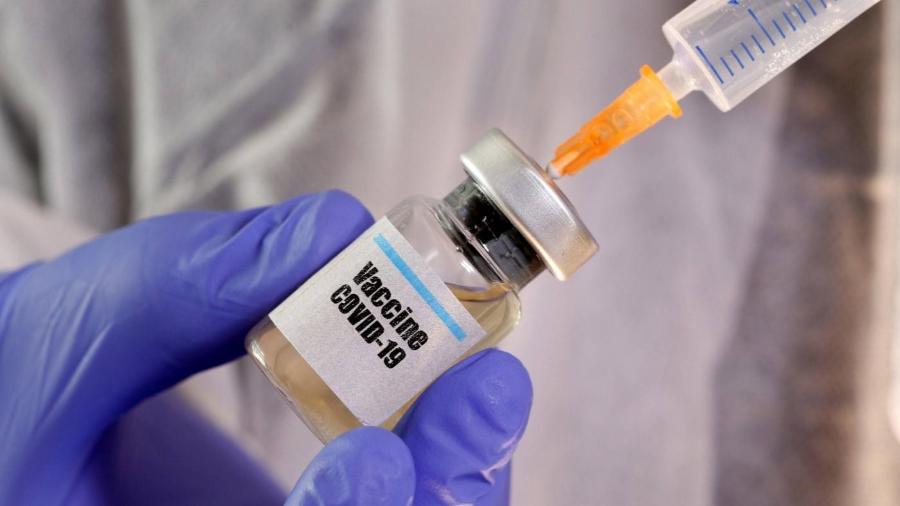
Cientistas de todo o mundo trabalham em mais de 200 projetos para produzir uma imunização eficaz contra o coronavírus. A OMS (Organização Mundial da Saúde) espera que, com sorte, até o final do ano, centenas de milhões de doses possam ser produzidas.
É um anúncio esperado pelo mundo todo e é uma questão de tempo: por hora, todas as esperanças estão voltadas para essa sigla: AZD 1222 - a tão esperada vacina contra o coronavírus, que já matou quase 500.000 mil pessoas. Sua eficácia ainda não foi comprovada, mas tudo indica que há razões para que seus resultados sejam positivos.
Desenvolvida pelo laboratório inglês AstraZeneca, ela já é alvo de um acordo de princípio com a França, a Alemanha, a Holanda e a Itália, que fizeram uma pré-encomenda de 400 milhões de doses. A última fase de testes contará com mais de 30.000 pessoas e o laboratório acredita que, em setembro, será possível saber se a imunização funciona ou não.
O Brasil participa dos testes e, com resultados favoráveis, ela poderá ser usada antes mesmo do fim do estudo, obtendo uma licença para "uso emergencial em situação de pandemia." A chamada vacina de Oxford utiliza um vírus inativado e teve seu código genético modificado. Ela começou a ser testada na semana passada em cerca de 5 mil profissionais da Saúde do Estado de S. Paulo.
Por enquanto, tudo indica que a covid-19 não vai desaparecer, mas se integrar à lista de vírus sazonais, como a gripe. Por isso, a vacina será provavelemente a única maneira de vencer a doença, mas muitas pessoas já se dizem reticentes à ideia de injetar uma imunização produzida a toque de caixa. Uma grande parte do longo processo consiste justamente em efetuar testes para controlar a segurança e os efeitos colaterais.
Normalmente, a fabricação de uma vacina leva entre 8 e 15 anos e Uma grande parte do longo processo consiste justamente em efetuar testes para controlar a segurança e os efeitos colaterais. É o que explica o professor Fréderic Tangy, diretor de inovação de vacinas do Instituto Pasteur, que também inicia testes clínicos com uma vacina a partir de julho.
A única exceção para essa regra é a gripe, mas se trata do mesmo produto, que é adaptado quando chega o inverno. No caso do coronavírus, cientistas, laboratórios e organismos de financiamento se mobilizaram para produzir tudo da estaca zero o mais rápido possível, o que por si só já é um feito científico.
Três fases de testes em humanos
Produzir uma vacina, explica Tangy, passa por muitas etapas: a primeira é a pesquisa acadêmica e médica, fundamental para entender a doença - como ela é transmitida, seus sintomas, e quais pessoas resistem à infecção. Os chamados assintomáticos possuem um sistema imunológico capaz de neutralizar um agente e são a chave para entender como o corpo se defende contra a doença.
A segunda etapa é criar um produto, a vacina em si, que seja de fabricação industrial simples, para que possa ser produzida com facilidade em grande escala e acessível a todos. "Paralelamente, fazemos os testes clínicos e demonstramos a eficácia do produto no homem. Claro que só testamos produtos que já demonstraram ser eficazes em modelos animais", explicou Tangy em entrevista ao programa "Priorité Santé", da RFI. Ele lembra que essa é uma regra ética: só podem ser testados em humanos agentes com grandes chances de sucesso e cuja toxicidade tenha sido avaliada nos animais.
Em seguida, os testes em humanos têm três fases. A diferença é que, na primeira, o produto é aplicado em poucas pessoas, para que sua inocuidade seja avaliada. Na fase dois, centenas de humanos, entre 300 e 400, recebem uma dose. Todos os possíveis efeitos colaterais, como febre, dor de cabeça ou diarreia, por exemplo, são listados. "Quando mais voluntários, mais teremos, estatisticamente, informações", diz o pesquisador francês.
Os cientistas medem a resposta imunitária, tirando sangue dos voluntários para observar se eles fabricam anticorpos e se eles são ativos,analisando também a resposta celular e imuno-histoquímica à vacina. O pesquisador francês esclarece que o estudo é adaptado em função da idade da população-alvo e do país, dependendo de onde a vacina será registrada.
"No fim, iniciamos a fase 3, com um grande número de voluntários, porque precisamos demonstrar que o produto é eficaz para proteger contra a doença. Por exemplo, no caso da Covid-19, vamos injetar um placebo em 10.000 pessoas e a vacina em outras 10.000 pessoas e contar, de três a seis meses depois, quem pegou a doença ou não", explica.
Competição e segurança
A rapidez para se obter uma imunização pode representar um risco para a segurança desses pacientes? É provável, na opinião do professor, que lembra que, no caso da SARS-CoV-2, muitos laboratórios pularam a etapa de testes no modelo animal, sem repetir as experiências. "O que me dá medo atualmente é que, se criamos uma vacina com efeitos colaterais graves, porque não foi suficientemente testada, isso será dramático, ainda mais em uma época de desconfiança em relação às vacinas", comenta.
Tangy também alerta para o risco de privilegiar o interesse econômico dos laboratórios. "É o risco que corremos, atualmente, com o novo desenvolvimento da vacina contra a covid-19. Todos os industriais esperam que ela seja anual, porque a epidemia corre o risco de voltar todos os anos", diz.
O professor francês lembra que as novas tecnologias de fabricação de vacinas requerem também estrutura de ponta. "São vacinas concebidas para países ricos, que podem pagar de US$ 150 ou até US$ 500 a dose, reembolsados pelo sistema de saúde. Uma parte do mundo será deixada de lado". A vacina deve ser bem um bem de utilidade pública, que deve ser acessível a todos, defende o cientista francês, e esse equilíbrio parece frágil no caso do coronavírus.













ID: {{comments.info.id}}
URL: {{comments.info.url}}
Ocorreu um erro ao carregar os comentários.
Por favor, tente novamente mais tarde.
{{comments.total}} Comentário
{{comments.total}} Comentários
Seja o primeiro a comentar
Essa discussão está encerrada
Não é possivel enviar novos comentários.
Essa área é exclusiva para você, assinante, ler e comentar.
Só assinantes do UOL podem comentar
Ainda não é assinante? Assine já.
Se você já é assinante do UOL, faça seu login.
O autor da mensagem, e não o UOL, é o responsável pelo comentário. Reserve um tempo para ler as Regras de Uso para comentários.